一、卤素原子怎样取代苯环侧链上的氢原子
光照下溴代物只发生在侧链的α-碳原子上的氢,铁粉催化条件下溴代则发生在苯环上的氢原子.卤族元素指周期系ⅦA族元素。
包括氟(F)、氯(Cl)、溴(Br)、碘(I)、砹(At),简称卤素。
它们在自然界都以典型的盐类存在 ,是成盐元素。
卤族元素的单质都是双原子分子,它们的物理性质的改变都是很有规律的,随着分子量的增大,卤素分子间的色散力逐渐增强,颜色变深,它们的熔点、沸点、密度、原子体积也依次递增。
卤素都有氧化性,氟单质的氧化性最强。
卤族元素和金属元素构成大量无机盐,此外,在有机合成等领域也发挥着重要的作用。
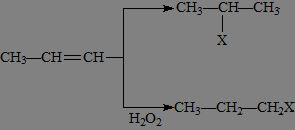
二、如何比较原子轨道能量高低?求大神指教
展开全部这个问题容易产生误解。
核外电子排布中所说的能量最低原理中的能量是特指轨道的能量(不考虑电子自旋对电子能量的影响)。
而更广义的能量最低原理中所说的能量是指任一系统的自身能量的总和(对于宏观系统即是内能)。
对于原子系统而言,广义的能量最低原理要求所有电子的能量(考虑电子自旋对能量的影响)总和最小。
因此狭义的能量最低原理和洪特规则甚至保里(泡利)原理都是广义的能量最低原理的具体要求。
反过来说如果不同时满足这三个具体要求,原子系统的总能量就不是最低,系统就处于不稳定的状态(即所谓的激发态)。
原子通常情况下都尽可能处于能量最低的状态(即所谓的基态),能量较高的激发态不是不可能存在,而是要存在的话需要外界输入能量,并且存在的时间极短。
不同轨道之间能量的差别较大,而电子自旋引起的能量差异较小,因此电子排布时,首先要满足狭义的能量最低原理(同时满足保里原理)。
例如2p轨道上有空位(有没有空位是保里原理说了算)时,电子不会排到3s或能量更高的轨道上去。
比方碳原子首先填充1s轨道2个电子,再填2s轨道2个电子,剩下的两个电子将排在2p轨道中。
至于这两个电子在2p轨道中怎么排就是洪特规则说了算(三个p轨道中的两个分别填充1个电子,且这两个电子自旋平行,这样才能使电子的总能量最低。
如果两个电子以自旋相反排在同一个p轨道中这样电子的总能量要比前一方式要高)。

三、氢原子平均质量是怎样测量出来的?
很多年来科学家一直以为空气是一种单一的物质。
随着欧洲文艺复兴,传统炼金术逐渐被制药与冶金业所取代。
有的化学家在实验中发现,把铁放在硫酸中会发生激烈的化学反应,冒出许多可以燃烧的气泡,似乎与普通的空气不太一样。
18世纪50年代,英国科学家卡文迪什发现,用铁、锌与稀硫酸和稀盐酸发生反应,生成一种不溶于水和碱液的气体,在与空气混合点燃时会发生剧烈爆鸣,爆鸣后瓶内有水珠出现,因此他给这种气体取名为“可燃气”。
这种气体有一个特别之处,当给猪的尿泡充入这种气体后会在空气中冉冉上升。
卡文迪什当时信奉燃素说,他一度以为自己发现了很多人梦寐以求的“燃素”,众多燃素说信奉者也都欣喜若狂,将其作为燃素具有负重量的重要依据。
卡文迪什最终测出“可燃气”的密度,发现虽然它比普通空气轻得多,但也有重量。
“可燃气”后来被法国化学家拉瓦锡改称为氢气。
1783年12月,人们首次搭乘绸布制作的氢气球飞上天空。
此后,充有氢气的载客飞艇一直沿用到20世纪30年代。
氢气还被广泛用于合成氨和甲醇,用于炼油厂中为石油脱硫,制备有机化合物溶剂和试剂,用于以动植物脂肪制取人造黄油等。
20世纪初,人们认识到氢气是一种双原子组成的分子,氢原子是所有元素中最轻的。
1904年,因发现电子而著名的英国科学家汤姆逊担任剑桥大学卡文迪什实验室主任。
他首次提出原子结构的模型,即原子是一个均匀的带正电荷的球体,里面飘浮着许多电子,电子所带电荷与球体所带的正电荷恰好相等,所以整个原子是中性的。
但原子失掉电子后又会如何呢?汤姆逊决定研究这一问题。
他将原先发现电子时所做的阴极射线实验重做了一遍,但这一回把仪器的高压电极反过来接,原来的阴极变为阳极,结果产生一束带正电荷的射线,汤姆逊称之为“阳极射线”。
接下来,汤姆逊测量阳极射线在电场和磁场的作用下发生的偏转,然后求出其中电荷和质量的比值。
为了进行比较,他在射线管内分别使用了纯净的氢气、氧气、氮气和氦气等。
结果发现,同阴极射线不同的是,阳极射线粒子的电荷和质量的比值随气体的不同而差异很大,这说明阳极射线是失去了电子的某种离子。
后来经过其他科学家的精密测量和计算,得出失去电子的氢离子,也就是氢原子核的质量是1.67*10^-24g,比电子的质量大1836倍。
因为电子质量很小,氢原子核的质量差不多就等于氢原子的质量。
以后,科学家们更深入地研究了氢的各种特性,确定了氢在整个地球和宇宙中的比例,虽然氢在地球总物质含量中只占0.9%,但却是整个宇宙中最丰富的物质,约占75%。
四、试比较氢原子中电子与原子核的静电力和万有引力的大小
库仑力 Fa = k*Q1*Q2/r^2 万有引力 Fb = G*M1*M2/r^2 Fa/Fb = k*Q1*Q2/(G*M1*M2) k = 9×10^9 牛顿 米^2 /库仑^2 Q1 = Q2 = 1.602 × 10^(-19) 库仑 G = 6.673×10^(-11)米^3/千克秒^2 M1 = 1.67×10^(-27)千克 M2 = 9.31×10^(-31)千克 r = 0.53 × 10^(-10) 米 代入算得 Fa/Fb = 2.22 × 10^39 即 静电力是万有引力的 10^39 倍 其中 Fb = 3.7×10^(-47) 牛顿 Fa = 8.2×10^(-8) 牛顿
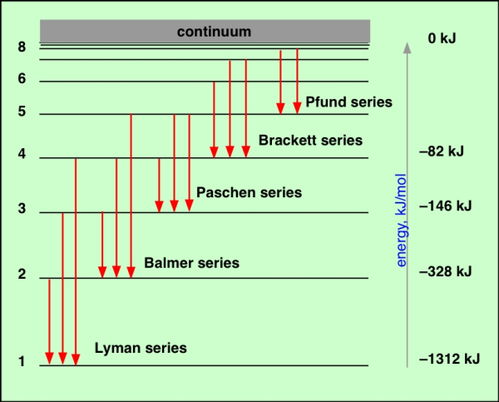
五、氢原子光谱的思考题
和标准谱对比
六、在核磁共振 氢谱图 中如何在图上看氢原子的个数比?如果用实例解析更好。
先确定比较特殊的H的大致出峰位置,再将该H定出个数(如目标分子所选特殊H 为1,则定之),然后在对其它峰进行积分, 其它峰自然会出现相对H 个数。
在与目标分子H个数相比对你应该是会积分的吧,这个和峰的面积有关。
在非溶剂的峰的面的比例,一般打HNMR是人家会帮你积分搞好,老干这事的人会找的认为是一个H,或两个H,三个H的峰,计算其他峰的面积与他相比较,当然也会出现多积分一倍或少了,但受到谱图的人是会看的懂的。
直接用软件分析出来,直接就可以看了!!LZ看来不是学化学的呀!!跨考??朋友可以到行业内专业的网站进行交流学习!分析测试百科网这块做得不错,气相、液相、质谱、光谱、波谱、药物分析、化学分析、食品分析。
这方面的专家比较多,基本上问题都能得到解答,有问题可去那提问,网址百度搜下就有。

七、怎样判断烃类物质中哪个氢活泼?
离官能团近的更活泼,越对称的越不活泼,氢原子越少的碳上氢原子突越活泼

参考文档
下载:如何比较氢原子能量值.pdf《股票锁仓后时间是多久》《行业暂停上市股票一般多久》《农业银行股票一般持有多久分红》下载:如何比较氢原子能量值.doc更多关于《如何比较氢原子能量值》的文档...声明:本文来自网络,不代表【股识吧】立场,转载请注明出处:https://www.gupiaozhishiba.com/chapter/34206494.html



